Arvematerialet til alle menneske er 99.9 prosent likt, men forskinga på variasjonen i den siste promillen reflekterer ikkje det etniske mangfaldet i befolkninga. Det kan gje negative konsekvensar for dei gruppene som ikkje er representert.
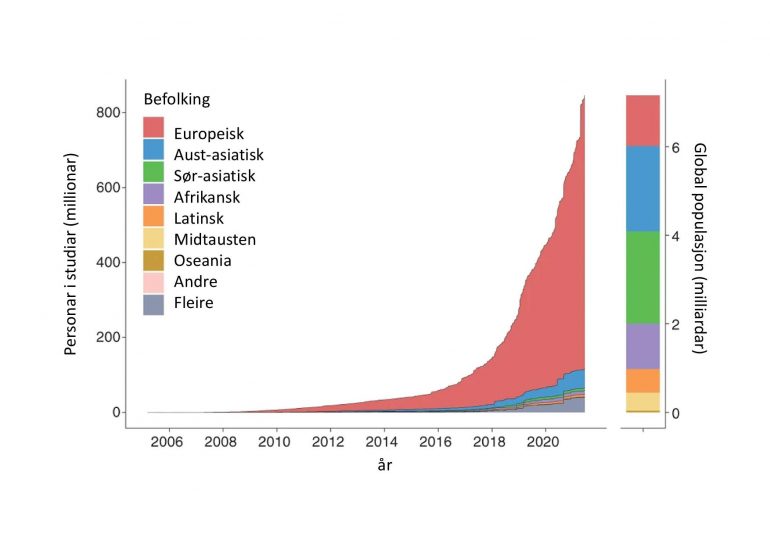
Nesten alle genetiske studiar er gjort på personar med europeisk opphav. Trass i at dette manglande mangfaldet i genetisk forsking har vore kjend lenge, har lite blitt gjort for å endre det. I 2021 var heile 86 prosent av alle genetiske studiar gjort på personar med europeisk opphav, ei forverring av tala frå 2016 då 81 prosent hadde europeisk opphav.
– Ei breiare og betre inkludering i genetiske studiar vil vere til nytte for alle, ikkje berre for dei gruppene som no er underrepresentert, seier professor Esperanza Diaz ved Institutt for global helse og samfunnsmedisin ved Universitet i Bergen. Diaz har forska på innvandrarhelse i fleire år og er òg leiar av det nyoppretta Pandemisenteret.

Historiske årsaker
Det manglande mangfaldet i genetisk forsking er ikkje unikt, og ein finn dei same kjenneteikna i anna medisinsk forsking. I ein kommentarartikkel i Nature Medicine peikar Segun Fatumo og kollegane på to grupper som er underrepresentert: personar frå låg- og mellominntektsland, og personar frå minoritetar og urfolk i alle land.
Ein viktig årsak til dette er manglande mangfald hjå dei som forskar. Diaz meiner at mangfald hjå dei som forskar gir gevinst for fleire.
– Tillit, god kommunikasjon og lettare involvering av minoritetsgruppene er nokre av fordelane. Vi veit at innvandrarar oftare vel fastlegar med innvandrarbakgrunn, sjølv om dei ikkje er frå dei same landa. I mi forskingsgruppe har vi sjeldan hatt problem med å rekruttere personar frå minoritetsgrupper, for vi har forskarar frå mange ulike land, seier ho.
Konsekvensar for helse
I tillegg til den kunnskapsmangelen det manglande mangfaldet i genetisk forsking førar til, vil den òg kunne gi ei rekke negative helsekonsekvensar for dei som er underrepresentert. Kunnskap om genetiske risikofaktorar og kvifor folk blir sjuke er allereie viktig, og vil bli enda meir sentralt i framtida. Til dømes er det meir og meir vanleg å nytte sokalla polygene risikoskår. Dette er algoritmar der ein nyttar kjennskap til ulike genvariantar ein veit er assosiert med sjukdom, saman med anna pasientinformasjon, til å rekne ut sjukdomsrisiko. Men genvariantar og sjukdom er ikkje den same hjå personar med ulikt genetisk opphav, noko som kan gje heilt feilaktige berekningar og dårlege helseval.
Auka sjukdomsforståing gir betre førebygging av sjukdom, og er og viktig for tidleg og presis diagnostisering når sjukdom oppstår. Og for at etniske minoritetar skal kunne ta del i gevinsten frå legemiddelutvikling og nye og betre behandlingstilbod, må desse gruppene også inkluderast i forsking og kliniske studiar. Innvandrar og etniske minoritetar har ofte dårlegare helse enn andre grupper, og om dei ikkje får ta del i den medisinske utviklinga vil dette kunne auke helseulikskapen ytterlegare.


Forsking i Noreg
– Svakheiter ved å nytte polygene risikoskår for til dømes hjartesjukdom er dei same i Noreg som i andre land. Slik dei genetiske studiane er i dag vil slike risikoskår kunne fungere godt for personar med europeisk opphav, men dårleg for personar med anna opphav, seier Kristian Hveem, leier for K.G. Jebsen-senteret for genetisk epidemiologi ved NTNU i Trondheim.
Kollegaen Brooke Wolford, postdoktor ved senteret, har jobba med statstikk og store genetiske datasett i både USA og i Noreg. Ho seier at løysinga må vere internasjonal.
– Det er naudsynt med store studiar med mange deltakarar for å klare å påvise samanhengar mellom genvariantar og sjukdom. Det er rett og slett for få personar i Noreg. Men slike data vert alltid betre om dei store internasjonale datasetta vert supplert med nasjonale data, seier Wolford.
Naudsynte tiltak
– Den manglande diversiteten i genetiske studiar er eit tema i fagmiljøa, mellom anna på store internasjonale kongressar. Noko av utfordringa er å få finansiering til store genetiske kartleggingsstudiar til dømes i Afrika. Slike store studiar er ofte offentlege-private samarbeid, der dei private aktørane ønskjer mest mogleg tilbake frå investeringane sine. Då er land med etablert infrastruktur og kompetanse meir freistande å investere i, seier Hveem.
Diaz meiner at tiltak på systemnivå vil kunne betre situasjonen i Noreg og at ein må vere særs eksplisitt og direkte for å få til endring, for desse tinga skjer ikkje av seg sjølv.
– Det må ein eigen strategi og handlingsplan for innvandrarhelse til. Alt for ofte tenkjer vi at folk frå innvandrargrupper er for vanskelege å nå, utan at vi tenkjer på kva for strukturar og system som gjer at det er sånn. Om dette ikkje adresserast har vi rett og slett ei form for institusjonell diskriminering. Eit døme er helseregistra våre, som med unntak av Kreftregisteret, ikkje har registrert innvandrarbakgrunn.
Frykta har vore at slik informasjon kunne misbrukast. Men pandemien har vist oss at slik informasjon kan vere heilt sentral for å kunne gi god helsehjelp, seier Diaz.
Det er mange fagmiljø som no ønskjer seg ein slik strategi. For genetikk er berre ein del av det store bildet, og for å redusere ulikskapen i helse krevjast det ei brei tilnærming, avsluttar ho.
Kjelder:
- Segun Fatumo et al. A roadmap to increase diversity in genomic studies. Nature Medicine, 2022, 1-8. https://doi.org/10.1038/s41591-021-01672-4
- Tina Hesman Saey. DNA databases are too white, so genetics doesn’t help everyone. How do we fix that? https://www.sciencenews.org/article/genetics-race-dna-databases-reference-genometoo-white
- Jocelyn Kaiser. NIH’s huge All of us genes and health study releases first 100 000 genomes https://www.science.org/content/article/nih-s-huge-all-us-genes-and-health-study-releases-first-100-000-genomes




