Med moderne genteknologi er drømmen om xenotransplantasjon, å transplantere organer fra andre arter inn i mennesker, nærmere virkelighet enn noen gang. Men de etiske problemstillingene består.
Det første dokumenterte tilfellet av xenotransplantasjon kom i 1905, da biter av en kanin-nyre ble operert inn i et fransk barn med nyresvikt. Siden da har blant annet sjimpansetestikler, lammenyrer og bavianhjerter blitt transplantert inn i mennesker, men uten suksess. Da den 57 år gamle hjertesyke amerikaneren David Bennett fikk et hjerte fra en genmodifisert gris 7. januar i år, var det verdens første vellykkede xenotransplantasjon. I flere uker fungerte hjertet fint, men etter hvert ble Bennett dårligere og han døde 8. mars.
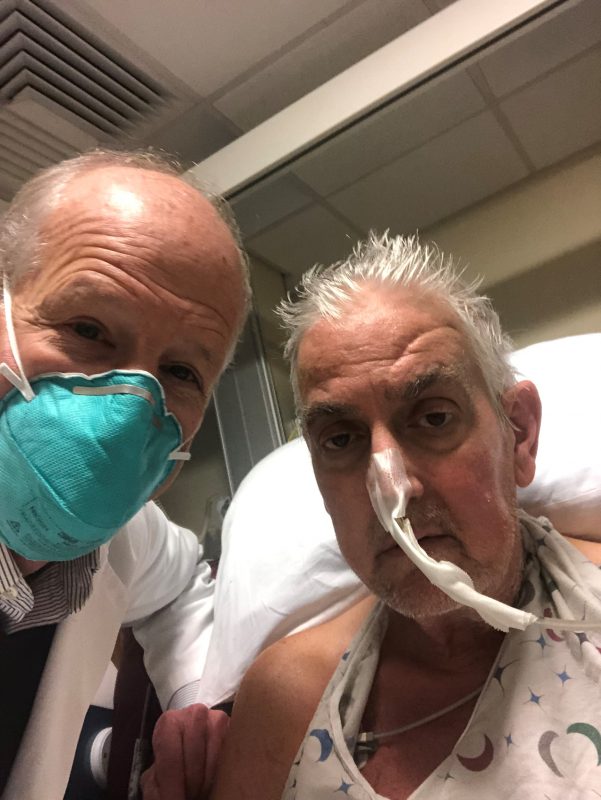
Medisinsk behov
Selv om mytologien rundt mennesker med organer og egenskaper fra dyr går tilbake til blant annet gresk mytologi, bygger moderne forskning på xenotransplantasjon på et helt reelt medisinsk problem: det er ikke nok menneskeorganer tilgjengelig. I Norge er det til enhver tid rundt 500 mennesker som venter på et nytt organ og flere av disse dør i køen.
Behovet for organer er stort, men det er tre store problemstillinger knyttet til xenotransplantasjon: organavstøting, virusinfeksjoner og etikk. Med moderne bioteknologi er vi i ferd med å løse de to første, mens de etiske problemstillingene forblir.
Avstøtning
Mange, inkludert Kong Harald, har fått operert inn en hjerteklaff fra gris som erstatning for en ødelagt hjerteklaff. Slike hjerteklaffer er dødt vev, og kroppen reagerer ikke på dem. Når et levende grisehjerte settes inn i en menneskekropp, vil derimot kroppen forsøke å støte fra seg det fremmede organet via en rekke ulike mekanismer. Mange av disse avstøtningsmekanismene skjer også i organdonasjon mellom mennesker, men et grisehjerte gir i tillegg en ekstra hyperakutt avstøtningsreaksjon. Reaksjonen skyldes at mennesker har antistoffer mot et sukkermolekyl på innsiden av griseblodårene. Disse antistoffene reagerer umiddelbart og i løpet av minutter vil en kaskade av blodpropper, betennelse og vevsdød ødelegge hjertet. Her kommer moderne genteknologi inn.
Grisehjertet som ble transplantert inn i David Bennett kom fra en gris med en rekke genetiske endringer som forhindrer en slik avstøtningsreaksjon. Forskere har i nesten 20 år brukt klassisk genmodifisering til å avle frem griser uten sukkermolekylet som trigger avstøtningen. Dette gjør de ved å klone frem griser uten et virksomt sukkerenzym. For å øke sannsynligheten for at grisehjertet blir akseptert av menneskekroppen er to andre sukkermolekyl skrudd av, og i tillegg er seks menneskegener satt inn. Disse er viktige for å kontrollere blodlevringen og dempe betennelses- og immunreaksjoner i kroppen. Og siden griser og grisehjerter kan bli mye større enn mennesker og menneskehjerter, er det også skrudd av et vekstreseptorgen slik at hjertet ikke skal vokse seg for stort.
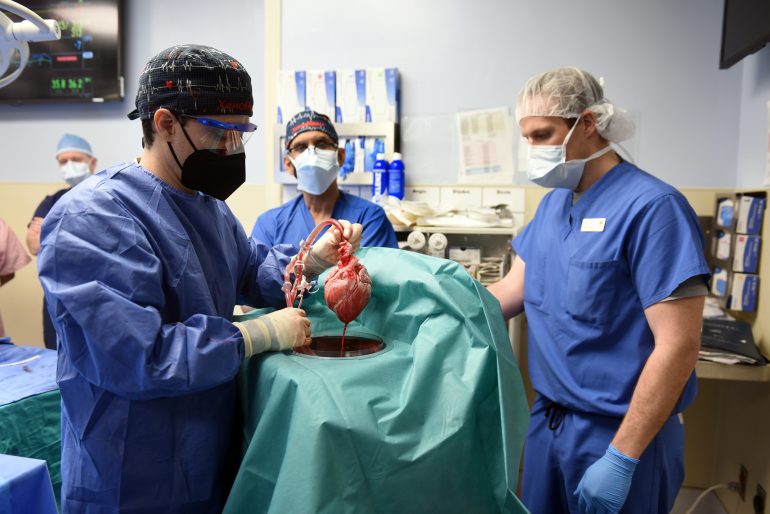
Akkurat hvilke genteknologiske metoder som er brukt til de andre endringene er ikke blitt bekreftet, men forskerne omtaler selv grisen hjertet stammer fra som genredigert. Mens tradisjonelle genmodifiseringsmetoder er upresise og gir liten mulighet til å målrette de genetiske endringene, kan de nye metodene for genredigering gjøre presise endringer på enkeltgener. Dermed kan forskere slå ut eller sette inn akkurat de genene de trenger for at griseorganer skal aksepteres av menneskekroppen. Det er allerede gjort flere vellykkede forsøk hvor grisenyrer har blitt transplantert til hjernedøde mennesker.
Virusinfeksjoner
Den andre store problemstillingen genteknologi kan løse er faren for virusinfeksjoner fra gris i mennesker som har fått griseorganer. At grisen ikke har hepatitt, influensa eller koronavirus kan man forsikre seg om ved hjelp av tester, men gris og andre dyr kan i tillegg ha såkalte endogene retrovirus. Dette er ikke levende virus, men gener fra gjennomgåtte virusinfeksjoner som er blitt del av grisens DNA. Frykten er at disse virusene skal våkne til liv i mennesker, og i verste fall skape pandemier med nye og ukjente virus.
I 2017 klarte forskere fra blant annet USA, Kina og Danmark å bruke genredigering til å slå av alle de 62 kjente retrovirusene i DNA-et til gris. Det er ikke kjent om organer modifisert med denne metoden har blitt satt inn i mennesker. Nye studier på mennesker som har fått transplantert insulinproduserende celler fra gris til behandling av diabetes, tyder på at faren for infeksjoner fra retrovirus kan være forholdsvis liten. Mottakere av dyreorganer vil måtte forplikte seg, og sine nærmeste, til strenge regler for testing, oppfølging og eventuelle karantener dersom de blir syke.
Etiske vurderinger
Genteknologi er altså i ferd med å gjøre xenotransplantasjon mulig, men de mange etiske spørsmålene står fortsatt ubesvarte. Noen handler om helt konkrete avveininger mellom fordeler og ulemper, mens andre er av mer filosofisk karakter. Gjør helsenytten for oss mennesker det akseptabelt å bruke dyr utelukkende som et middel? Er risikoen for virusinfeksjoner så liten at den kan tolereres? Må de som har fått et dyreorgan informere sine nærmeste, sine seksualpartnere og sine pleiere om en teoretisk fare for infeksjon? Og vil xenotransplantasjon gjøre noe med vår identitet – er en person med et dyreorgan litt mindre menneske enn alle oss andre?
***
Du kan høre mer om xenotransplantasjon og organdonasjon i Biotekpodden, hvor transplantasjonskirurg Pål-Dag Line ved Rikshospitalet er gjest.
Kilder:
www.nytimes.com/2022/01/10/health/heart-transplant-pig-bennett.html
www.science.org/doi/10.1126/science.aan4187
onlinelibrary.wiley.com/doi/full/10.1111/ajt.16930
www.forskningsetikk.no/ressurser/fbib/forskning-samfunn/xenotransplantasjon/




